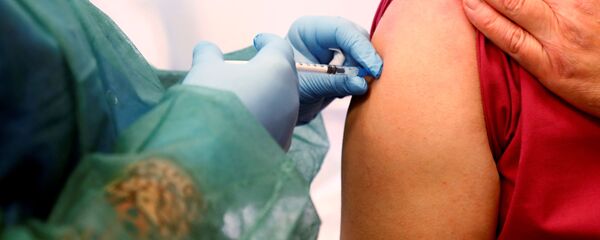
RĪGA, 19. janvāris - Sputnik. Decembrī internetā parādījās dati par "Pfizer-BioNTech" vakcīnas apstiprināšanu, smelti no Eiropas zaļu aģentūrai (EZA) nozagtajiem dokumentiem, ziņo franču izdevums Le Monde, kura raksta tulkojumu publicē Inosmi.ru.
Le Monde izdevies iegūt un publicēt dažas ziņas no noslepenoto dokumentu paketes, ko 2020. gada 9. decembrī Eiropas zāļu aģentūrai nozaga nezināmas personas. Ar dokumentiem iepazinās Eiropas žurnālistu komanda.
Mapē iekļautas 20 nodaļas, kas galvenokārt attiecas uz "Pfizer-BioNTech" vakcīnas materiāliem. Starp dokumentiem ir aģentūras atbildīgo darbinieku 19 vēstules, kas nosūtītas no 10. līdz 25. novembrim. Ar dažām to vidū "manipulējuši" hakeri, vēsta EZA komunikē no 15. janvāra. Tomēr sarunā ar "Le Mond" aģentūra atzina, ka "publicētās elektroniskās vēstules atspoguļo tālaika problēmas un diskusijas".
Piecas elektroniskās vēstules, kas nosūtītas daudziem adresātiem (tādējādi samazinās varbūtība, ka tās pakļautas manipulācijām), ļauj spriest par spiedienu, ar ko saskārās aģentūra – tā mērķis bija paātrināt pirmās Covid-19 vakcīnas apstiprināšanas procesu.
Piemēram, 12. novembra sarakstē viens no EZA darbiniekiem stāsta par sarunu ar ES veselības komisāri Stellu Kirjakidu (Stella Kyriakides). Uzstājot, "lai visas Eiropas valstis vienlaikus saņemtu vakcīnu", Kirjakidu arī uzsvēra, cik svarīgi ir "neforsēt" valstu nacionālo procedūru piemērošanu, jo tas novedīšot pie kavēkļiem preparāta apstiprinājuma procesā. Saskaņā ar ES direktīvu, epidēmijas gadījumā valstīm ir tiesības izmantot ārstniecības līdzekļus, ko nav apstiprinājusi EZA.
19. novembrī viens no augstākajiem EZA darbiniekiem min selektoru sanāksmi ar Eiropas Komisiju, kas norisinājās "diezgan saspringtā, reizēm pat nepatīkamā gaisotnē. Gaisotne sniedz priekšstatu par to, ar ko var saskarties EZA, ja cerības neattaisnosies, neatkarīgi no tā, vai tās ir reālistiskas vai ne."
Nākamajā dienā sarakstē ar Dānijas zāļu aģentūru tas pats ierēdnis atzina, ka viņam bijis negaidīts Eiropas Komisijas priekšsēdētājas Urzulas fon der Leienas (Ursula von der Leyen) paziņojums, kurā "skaidri nosauktas divas vakcīnas, kuras varēs saņemt apstiprinājumu līdz gada beigām ["Pfizer-BioNTech" un "Moderna"]. Ar abiem preparātiem joprojām ir problēmas," uzsvēra ierēdnis.
Par šīm "problēmām" ir runa pārējos decembrī nozagtajos dokumentos. Šī iemesla dēļ aģentūrai neradās aizdomas par manipulācijām. It īpaši runa ir par problēmām ar "Pfizer-BioNTech" vakcīnu.
Konstatēts, ka novembrī Eiropas aģentūra noformulējusi trīs "pamatiebildumus" pret šo vakcīnu:
- dažiem ražošanas laukumiem nav apstiprināta piekrišana;
- datu trūkums par vakcīnas komerciālajām partijām;
- un – pats svarīgākais – konstatētas atšķirības kvalitātē starp vakcīnas komerciālajām partijām un tām, kas izmantotas klīniskajās pārbaudēs.
Pēdējais punkts izraisīja vislielākās pētnieku bažas, kas nodarbojās ar vakcīnas kvalitātes novērtējumu.
"Klupšanas akmens"
Patiešām, pārejas posmā no klīniskajām pārbaudēm pie komerciālās ražošanas stadijas, nācās mainīt ražošanas procesu un ieguldīt līdzekļus jaunās rūpnīcās. Ar šīm izmaiņām skaidrojamas atšķirības vakcīnu sastāvā, it īpaši RNS integritātes līmeņa samazināšana. RNS ir būtisks vakcīnas elements, kas veicina vīrusa dzeloņveida olbaltumvielas sintēzi pēc tās ievadīšanas šūnās. Tā "apmāca" imūnsistēmu atpazīt patogēnu un neitralizēt to. RNS integritāte vakcīnās, kas tika izmantotas klīniskajos izmēģinajumos, sasniedza 69%-81%, proti, tā bija pilna ķēde, kas ļāva sintezēt dzeloņveida olbaltumvielu. Savukārt datos par jauno ražošanas līniju partijām atspoguļoti zemāki rādītāji: vidēji 59%. Dažās partijās RNS saturs sasniedza vien 51%-52%. Tas bija "klupšanas akmens", par ko ziņoja EZA 23. novembrī.
Rodas jautājums, vai zemāks RNS līmenis var ietekmēt ne tikai vakcīnas lietošanas efektivitāti, bet arī tās drošību. Zemāks RNS integritātes līmenis var liecināt par lielāku piemaisījumu skaitu, galvenokārt – nošķelto RNS skaitu. "Šajā produkcijā mēs bieži sastapāmies ar nedaudz īsākiem vai nedaudz garākiem RNS. Filtrēšana notiek, ņemot vērā molekulas lielumu, taču ar lieliem apjomiem process tiek apgrūtināts," komentē informāciju Stīvs Paskolo (Steve Pascolo), Cīrihes universitātes slimnīcas pētnieks, kurš jau divdesmit gadus strādā pie RNS vakcīnām. (Būdams CureVac līdzdibinātājs, 2000. gadā viņš pameta šo uzņēmumu un pašlaik veic projektus kopā ar BioNTech). Šīs saīsinātās RNS acīmredzot nevar veicināt dzeloņveida olbaltumvielu sintēzi. Tomēr dati, ko kompānija iesniedza EZA, norāda: olbaltumvielas tiek sintezētas RNS līmenī, kas vienāds 62%. " BioNTech pirmo pārbaužu gaitā imūnreakcija radās ar vienu RNS mikrogramu, — skaidro Stīvs Paskolo, — Plānots, ka vakcīnā būs 30 mikrogrami, tātad ir rezerve."
Līdzīgs viedoklis ir arī ASV Pārtikas produktu un medikamentu kvalitātes sanitārās uzraudzības pārvaldei, ar kuru tāpat kontaktējās EZA. Pārvaldē "jautājums par RNS saturu netika uzskatīts par nopietnu problēmu", pauda EZA ierēdnis 23. novembra elektroniskā vēstulē.
Patiesībā, šajā ziņojumā ir teikts, ka šīs ražošanas un kvalitātes kontroles problēmas nav attiecināmas uz steidzamas apstiprināšanas procedūrām (ASV, Kanādā un Apvienotajā Karalistē). Patiesībā tā nav vakcīnas atļauja, - tā ir atļauja preparāta pagaidu lietošanai. Pagaidu atļauja vakcīnas ieviešanai tirgū, ko centās saņemt EZA, uzliek vairāk ierobežojumu. Tādējādi rodas nepieciešamība "saskaņot ar EZA, Valsts sanitārās uzraudzības un Kanādas aģentūras vispārējām prasībām, lai izvairītos no varbūtības, ka kāds reģions saņems nederīgu materiālu," pēc dažām dienām tika paziņots vienā no elektroniskajām vēstulēm.
"Galvenais iebildums"
26. novembrī BioNTech un Pfizer radās iespēja atbildēt uz EZA iebildumiem. Kompānijas informēja par pārbaudēm dažādās ražotnēs un piedāvāja paaugstināt RNK satura minimālo līmeni līdz 60% ražošanas sākumposmos, lai izvairītos no tā samazināšanās galaproduktā līdz līmenim, kas mazāks par 50%. Šķiet, minētais kritērijs tika pieņemts visos saskaņošanā izmantotajos dokumentos. Savā ziņojumā "Comirnaty" vakcīnas ražotāji apgalvo, ka atšķirības RNK daudzumā "nedrīkst ietekmēt" nedz produkcijas efektivitāti, nedz drošību. Dažas no šīm partijām jau izmantotas klīnisko pārbaužu laikā.
Tomēr šie dati, šķiet, nav pārliecinājuši Eiropas aģentūru, jo pēdējie dokumenti un pieejamie ziņojumi neļauj ignorēt "galveno iebildumu". To apliecina EZA un ražotāju elektroniskās sarakstes ekrānuzņēmums. "Šīs problēmas tiek uzskatītas par būtiskām, it īpaši produkta tipa inovatīva rakstura un ierobežotas pieredzes kontekstā. Tāpēc ir jāpiemēro stingrāka kontroles stratēģija." Viens no pēdējiem pieejamajiem ziņojumiem liecina, ka ražošanas procesu korekcija ļauj atjaunot integritātes līmeni līdz aptuveni 75%, kas ir salīdzināms ar klīnisko pārbaužu laikā izmantotajiem paraugiem.
Trīs dienas vēlāk, 3. decembrī, The Wall Street Journal publicēja rakstu par problēmu ar vakcīnas Pfizer ražošanu. "Dažās partijās izejvielu kvalitāte neatbilst normām. Mēs esam novērsuši problēmu, bet mums pietrūka laika nodrošināt šajā gadā plānotās piegādes," stāsta "cilvēks, kurš tieši piedalās vakcīnas Pfizer izstrādāšanā".
Vai šeit ir kāda saistība? Kompānija Pfizer atteicās komentēt situāciju, balstoties vien uz EZA kiberuzbrukuma izmeklēšanu, kas joprojām turpinās. Piektdien, 15. janvārī, BioNTech un Pfizer atkal ziņoja par aizkavēšanos ar piegādēm, aizbildinoties ar darbiem Beļģijas rūpnīcā Pursā.
Eiropas aģentūrā apstiprināja, ka vēlāk kvalitātes problēmu izdevies atrisināt. "Kompānijai izdevies atrisināt problēmas, kā arī sniegt informāciju un nepieciešamos datus, kas ļauj EZA pieņemt pozitīvu lēmumu par vakcīnu". Aģentūra apliecināja, ka pašreizējās tehniskās prasības attiecībā uz RNS līmeni "uzskatāmas par zinātniski pamatotām un pieņemamām".
Piemēram, aģentūra uzsver, ka diez vai saīsinātas RNS molekulas var veicināt proteīna vai peptīda veidošanos, tādējādi izraisot nevēlamas sekas. "Par spīti steidzamībai, visā Eiropas Savienībā vienmēr bija sapratne par to, ka augsto kvalitātes standartu jautājumos nevar būt nekādu kompromisu un jebkuriem ieteikumiem jābūt balstītiem vienīgi uz pārliecinošiem zinātniskiem pierādījumiem, kvalitātes drošību un vakcīnas efektivitāti," apgalvo EZA. Eiropas Komisijā uz mūsu jautājumiem arī atbildēja, ka šīs diskusijas "nekad nav kaitējušas aģentūras neatkarībai un nekādā ziņā nav kompromitējušas EZA lēmumu objektivitāti par vakcīnu un citu zāļu līdzekļu izvērtēšanu."
Krievu vai rusofilu pēdas
Joprojām nav zināms, kas varētu būt saistīts ar hakeru neseno uzbrukuma. Nozagtie dati parādījās torrentu vietnē "Rutor", kur "Ru" nozīmē "Krievija", bet "tor" - tīmekļa pārlūkprogramma, kas ļauj anonīmi lasīt vietnes internetā (pārlūkprogramma Tor nav saistīta ar Krieviju tika izstrādāta ASV JKS – red. piez.). Tas var kalpot par labu versijai, ka hakeris ir no Krievijas vai atbalsta to. "Līdzīgu uzlaušanas un datu zagšanas taktiku, kam seko to noplūde, jau ir lietojuši Krievijas hakeri (Guccifer 2.0, jeb Pasaules antidopinga aģentūras lieta), stāsta Žans Mišels Doans (Jean-Michel Doan), kompānijas "Sekoia" speciālists, kas nodarbojas ar kiberdrošības jautājumiem.
Turklāt ir grūti izslēgt versiju par rūpniecisko kiberspiegošanu, it īpaši ņemot vērā, ka, izvēloties dokumentus, noziedznieki orientējās tieši uz Pfizer. Uz to norāda arī failam piešķirtais virsraksts – "Vērienīgas krāpšanas ar vakcīnu Pfizer pierādījumi." Bet kā tad ir ar vakcinācijas nīdēju grupu, kas mēģināja diskreditēt vakcīnas? "Maz ticams, ka hakeris - vakcīnu nīdējs publicēs datus ne īpaši populārā tīmekļa vietnē, kuras specialitāte ir pirātisms," komentē Žans Mišels Doans.
Tikmēr fakti ir tādi: EZA pilnībā apstiprināja Pfizer-BioNTech vakcīnu 2020. gada 21. decembrī, trīs nedēļas pēc apstiprināšanas Lielbritānijā un divas nedēļas pēc apstiprināšanas Savienotajās Valstīs. tātad EZA, par spīti visam, bija vajadzīgs zināms laiks, lai atrisinātu problēmas. Eiropas Komisija norādīja, ka tāda aizkavēšanās nav pieļaujama – par to liecina sarakste no 19. novembra: "Lai ko mēs darītu, paātrinot saskaņošanas procesu (ar citām institūcijām) vai veicot to nepieciešamajos termiņos, lai iegūtu precīzas garantijas (…), EZA būs jāsaskaras ar jautājumiem un kritiku no dažādām pusēm (Eiropas Komisija, ES dalībvalstis, Eiropas Parlaments, mediji un sabiedrība)," teikts aģentūras augstā ranga ierēdņa paziņojumā. Viņš nevarēja prognozēt, ka līdztekus aģentūrai būs jātiek galā arī ar kiberuzbrukumu.